先日開催された土木研究所主催の共同研究報告会にてこの論文を初めて知りました。技術的にとても面白い内容だったので解説したいと思います。
ステベクスから環境DNAを抽出と精製のプロトコルの再検討(Part1)とPCR阻害(Part2)について述べています。実験を通して検出種数や感度について疑問に思われている方々の手助けになれば幸いです@しばた
(書いていて長くなったので2本立てにします。)
Sterivexフィルターを使用した環境DNAの抽出・精製・測定のための改良されたプロトコルの野外適用
この記事の内容
論文の要約
- ステリべクスを使った抽出法で既存の確立された方法と比較して、環境DNAの収量を12-16倍に改善
- 抽出と精製効率を回収率として評価するためにサンプルに内部標準DNAを添加
- タンパク質ベースの添加剤を使用して、試薬にTakaraProbe qPCR Mixを使用すると阻害がかかるようなサンプルでも分析の堅牢性が向上(TaqMan Environmental MasterMix 2.0とも比較)
- さらに阻害がかかるようなサンプルにはQiiagen PowerClean ProCeanupキットによる精製が必要な場合もあったが思ったより回収率は低かった(平均 33%)
抽出やPCR阻害についての簡単な説明
1. 一般的な環境DNAの抽出方法
環境DNAマニュアル v2.2ではCytiva(Whatman)のGF/FフィルターとSterivex-HV(SVHV010RS)の2種類のろ過方法があります。
それに伴い抽出法もサリベットやスピンカラムを使うものや、ステリべクスから直接抽出する方法など2,3通りあります。
両ろ過・抽出法とも一長一短であることから、それぞれの手法がマニュアルに記載されています。
サリベットを使ったGF/Fフィルターからの抽出法は以下のようなイメージです。
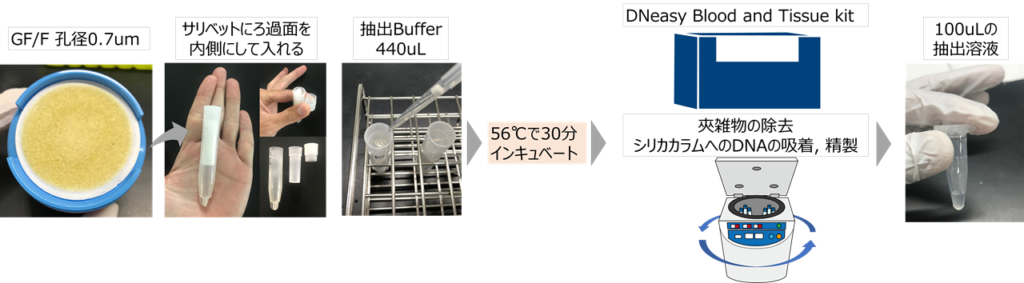
サリベットの大きさが15mLチューブのスケールなので、1サンプルが複数のフィルターでろ過せざるを得なくてもサリベット1本で済むはずです。欠点としては、マイクロチューブ用のロータでは処理できないので少し大きめのチューブ用のロータを使わないといけません。なので1回の処理量はスピンカラムと比較して少なくなります。
スピンカラムを使ったGF/Fフィルターからの抽出法は以下のようなイメージです。

スピンカラムは2mLチューブの程度の大きさなのでマイクロチューブ用のロータで抽出を進めることができます。なので1回で抽出できるサンプル数もサリベットよりは多く処理できます。欠点は1サンプルが複数枚のフィルターになってしまった場合、複数のチューブを使用する必要があります。
ちなみに私は普段この方法を使っています。
ステリべクスからのDNA抽出法は抽出法は以下のようなイメージです。
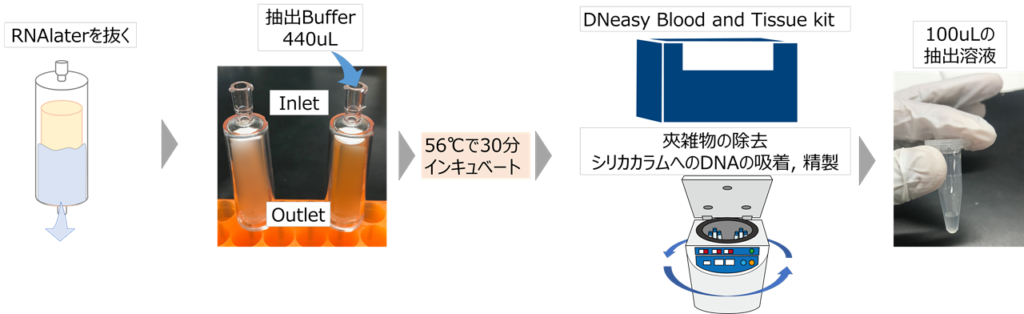
ステリべクスはGF/Fと素材と孔径が異なります。孔径は2種類あり、0.45umはフィルターの素材がPVDF(フッ化ポリビニリデン)、0.22umはPVDFとPES(ポリエーテルスルホン)です。
フィルターの素材と性質はCytivaのページが分かりやすいと思います。
マニュアルに記載されていない抽出法
千葉県立博物館の宮先生を含むグループの論文(Kawato et al.2021)では、マニュアル記載の方法とは少し異なる方法でステリべクスからDNAの抽出を行っていました。

上記ようなステリベクスを分解して抽出する方法は、海外の研究でよく見ます。
マニュアルと異なるのは、フィルターを分割して処理しており、通常1サンプル440uLで抽出を進めていくところを、その倍量の溶出液で溶出している点と、フィルターを細切れにして処理している点でしょうか。また、最終溶出も200uLです。
この方法でも確か抽出効率が上がっていたような覚えがありますが、ステリベクスの分解はちょっとコンタミのリスクも高まるので私は様子見してました。
フィルターから環境DNAを抽出するステップは、PCRと違って同じサンプルでやり直すことができないので、一番処理を注意しないといけません。
私が抽出ステップで重要だなと考えているのは
- 煩雑な作業がなくコンタミネーションのリスクが低い
- 遺伝子解析に使う一般的な分析機器で作業を進めることができる
- 多量のサンプルも1回の作業で処理可能(12サンプル〜)
- 汎用的な試薬を使用している
- 一部自動化もできる
ことです。
作業寄りな内容ですが、ここら辺が抜けていると環境DNA分析の良さである多量サンプルを捌けなかったり、高い機材や試薬を買い足したりしないといけなるような気がします。
2. PCR阻害とは?
PCRはポリメラーゼ連鎖反応と呼ばれるDNAを増幅させるプロセスです。M-hubのページが分かりやすいです。
ポリメラーゼ連鎖反応なのでPCRではポリメラーゼ(=核酸の合成酵素)を使います。合成酵素の活性が直接的または間接的に阻害されることをPCR阻害と言ったりします。
環境DNA分析で問題になりそうなPCR阻害物質はフミン酸やフルボ酸、タンニン酸などの植物に由来するものや、ヘマチン(血液生物)でしょうか。ヘマチン以外はどれもつ常に天然に存在しそうなのでこれらの複合的な要因を回避できる堅牢なPCRプロトコルが必要になると思います。
Uchii et al.2019では環境DNA分析の検出と定量化のためのPCR試薬の阻害体制の評価をしています。フミン酸、フルボ酸、タンニン酸に対して、以下のPCR試薬の阻害耐性評価をしています(選択された理由も記載)。
- TaqMan Gene Expression Master Mix(GMM)
- 一般的な環境DNAの研究で使用されているため
- TaqMan Environmental Master Mix 2.0(EMM)
- 一般的な環境DNA研究で使用されており、PCR阻害に対して耐性が高い(Jane et al.2015)
- TaqMan Fast Advanced Master Mix(FMM)
- いくつかの環境DNA研究で使用されているため(Uchii et al.2017, etc…)
- TaqPath qPCR Master Mix, CG (TMM)
- PCR阻害剤耐性が高く、キャリーオーバーコンタミネーションを防止するための(UNG)が含まれているため(UNGを含まないEMMより用途としてはいい?)
- KAPA3G Plant PCR Kit (K3G)
- リアルタイムPCR用には設計されていないが、植物由来の阻害に高い耐性を持つポリメラーゼが含まれているため
- Probe qPCR Mix (PQM)
- PCR阻害耐性が向上し、上記5つとは異なるポリメラーゼを使用しているため
評価の結果、
- 阻害耐性試薬でないGMM, FMMは阻害耐性試薬と比較して、フミン酸とタンニン酸に対する耐性が低かった
- 過去の研究で阻害が確認されているフィールドサンプルに対して阻害耐性のあるいくつかの酵素を使って検出を行ったところ結果が改善した。
- 阻害耐性試薬もそれぞれ得意不得意がある
といった感じです。
Minegishi et al.2019は本記事の論文と同チームの人が研究に取り組んでおり、やはりこちらでもPCR阻害に関する対処が必要だったみたいです。
DNeasy Blood and Tissue kitで抽出しただけでは阻害が強いため、Zymo Research OneStep PCR Inhibitor Removal kitとDNeasy PowerClean Cleanup Kitのそれぞれで精製し、希釈とポリメラーゼを工夫したり、BSAを添加するなどして、阻害のかかるサンプルに対して最適なプロトコルを見つけています。
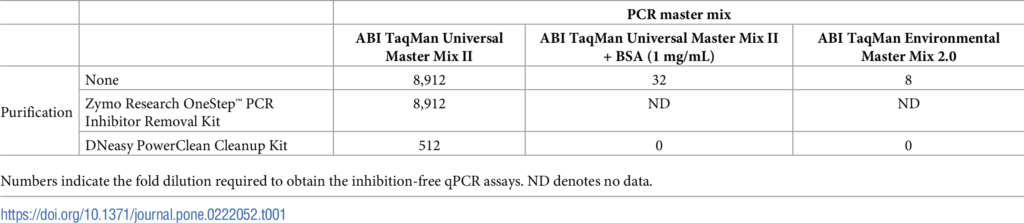
上記2本の論文でもわかる通り、環境DNA分析で問題となるPCR阻害はかなり厄介でかつ、統一した対処法がまだ確立されていません。
私が普段行っているのはDNeasy Blood and Tissue kitで抽出したDNA溶液をAmpureで精製する方法です。多数のサンプルを一気に処理できる点や、NGSの処理工程で使うので精製キットを追加で購入する必要もなく濃縮もかけれたりするので多用しています。
では、論文の本筋に移りたいと思います。
やったこと
本論文は以下の二つ検証をしています。
- 水槽水を用いた環境DNAの抽出と精製効率について
- 改変したプロトコルをフィールドサンプルに適用してみる
1.水槽実験による抽出と精製効率の検証
1-1. 水サンプルのろ過
実験系はFig.1を参考にすると分かりやすいです。ステリべクス(孔径0.45μm : Millipore SVHV010RS)で水槽水をそのままと10倍に希釈したものをれぞれ1L吸引ろ過しています。ろ過後はマニュアルに記載通り1.6mLのRNAlaterをインレットから注入して-20℃で保管しました。
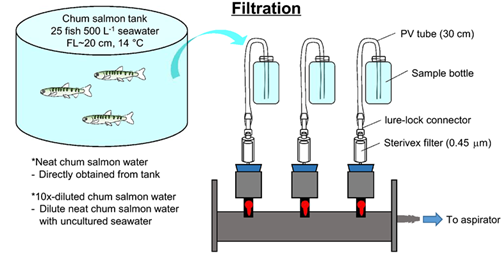
1-1-1. 環境DNAの抽出と精製
ステリべクスに添加したRNAlaterを解凍したのち、Outletから吸引して取り出しています。
抽出は以下の3通りの方法を試しています。
- 環境DNAマニュアル記載法
- 環境DNAマニュアルの約4倍の溶出バッファーをインレット側から添加
- 環境DNAマニュアルの約4倍の溶出バッファーをアウトレット側から添加
インキュベートはどのプロトコルも56℃で30分です。
インキュベート後はステリベクスのOutlet側を下に向けて、50mLチューブに取り付けられたスピンカラム(maxi spin)の上?にステリベクスをセットして、2500gで10分間遠心して抽出液を取り出しています。
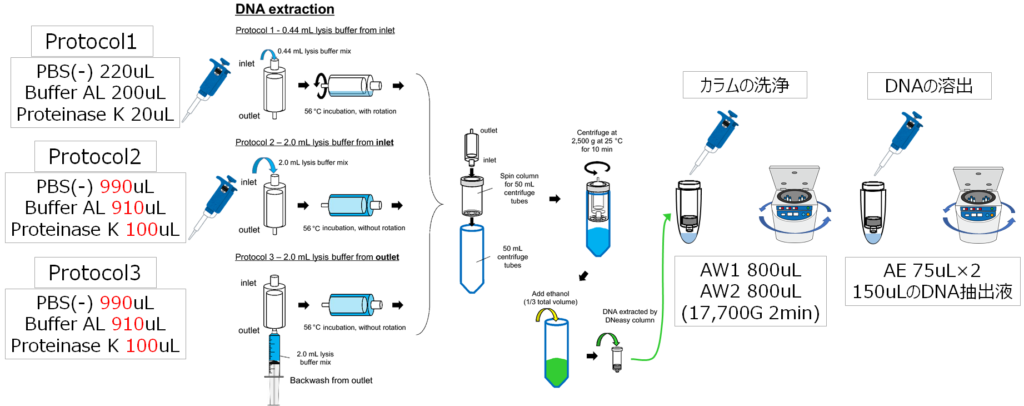
遠心で取り出した抽出液にProtocol1は環境DNAマニュアル通りの200uL, Protocol2,3は最終容量の1/3である1mLの99.5%エタノールを添加して、DNeasy Blood and Tissue kitに付属のカラムに吸引ろ過しています。
そのあとAW1とAW2でカラムに残る夾雑物を遠心ろ過洗浄し、最後に75uLのAE Bufferを2回カラムに通して計150uLのDNA抽出液を作成しました。
抽出液はQiagen DNeasy PowerClean Pro Cleanup Kitで精製しています。
また、抽出効率のテストのために同じステリべクスカートリッジを3回抽出しています。
1-1-2. 各プロトコル比較の結果
下記図はそれぞれのプロトコルで3回連続で抽出した抽出液をシロサケの検出系で定量PCRした時の定量値です。左からProtocl1, 2, 3となってます。
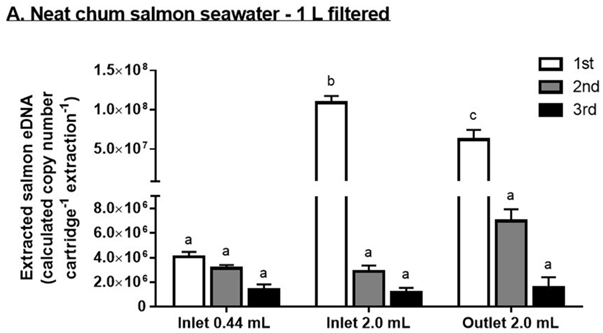
Protocol1(環境DNAに記載のプロトコル)は1,2回目ともほぼ同様の収量で、3回目は1回目の約1/3の収量でした(上記図A)。
Protocol2(インレットから抽出液を2mL注入)では、1回目がProtocol1と比較して、27倍の収量で、2,3回目はProtocol1と同様の収量でした。
Protocol3(アウトレットから抽出液を逆噴射)では、1回目がProtocol1と比較して、16倍の収量でしたがProtoclo2と比較すると43%少なかったです。2回目はProtocol2の2回目と比較して2倍の収量が得られました。
各プロトコルの抽出液の総DNA量を定量すると、
- Protocol1 : 189.3 ± 112.0 ng
- Protocol2 : 1183.3 ± 112.0 ng
- Protocol3 : 1183.3 ± 86.6 ng
となっており、明らかにマニュアル記載のプロトコルよりDNAの収量が多いようです。
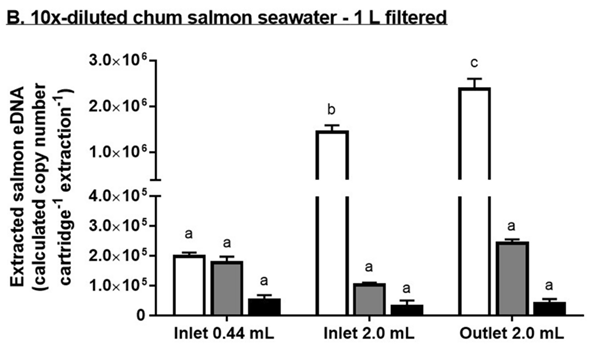
水槽水を10倍に希釈して濾過した処理系では、そのままろ過した実験系で得られた環境DNAの収量と比較してProtocol1, 2, 3はそれぞれ、4.8%、1.3%、および3.8%でした。
Protocol1の1,2回目の抽出ではほぼ同様の収量で3回目は1/4の量まで減りました。
Protocol2では1回目の環境DNAの収量がProtocol1の7倍の収量でしたが、2,3回目はProtocol1の半分程度となりました。
Protocol3では1回目の環境DNAの収量が有意に高く、2,3回目はProtocol1と同様でした。
各プロトコルの抽出液の総DNA量を定量すると、
- 392.0±33.2 ng
- 401.3±37.8 ng
- 682.0±35.5 ng
となっており、水槽水をそのまま使用した系の結果と比べると、各プロトコル間の総DNA量の差が少なくなっていました。
1-2-1.DNeasyのカラムのDNA保持能の検討
1-1の実験でInputされるDNA量が多い場合、アウトレット側から注入するプロトコルで抽出効率が低いことが分かりました。
この原因としてDNeasyのカラムのサンプルDNAで飽和して結合ステップの段階で保持されずに落ちてしまっている可能性があることが考えらます。
上記疑問を解消するため、2Lの水槽水と10倍希釈した1Lの水槽水をそれぞれ、高濃度群と低濃度群としてそれぞれでカラムの保持能力の検証をしました。
抽出はProtocol3(アウトレットから抽出液を逆噴射)の方法で行い、DNeasyのカラムを連結させて濾過する事で、Upperで保持しきれずに通過したDNAをLowerでキャッチするようにしました。
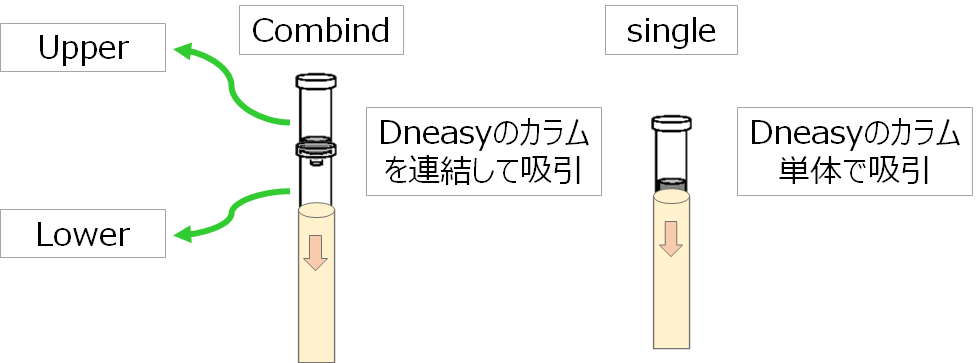
1-2-2. カラム保持能の検証結果
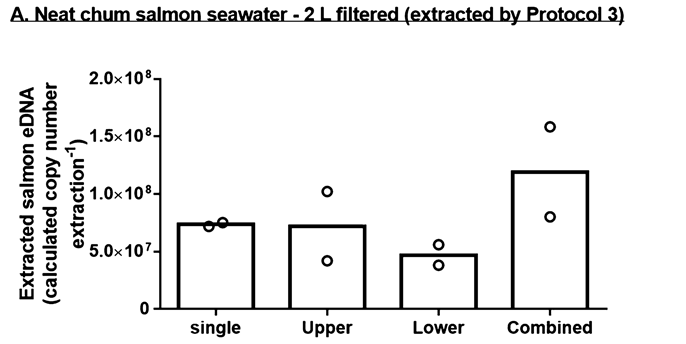
水槽水を2Lろ過した系の場合、DNeasyのカラムを連結させてそれぞれで抽出したUpperとLowerは単体で抽出したsingleと同等の値を示しました。
つまり、Input量が多いとDNeasyのカラムのDNA保持能を超えてDNAが通過してしまう可能性がある事を指してます。
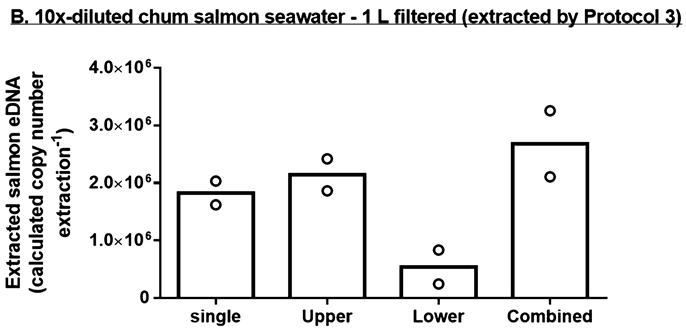
水槽水を10倍希釈て1Lろ過した系においても、Lowerで検出されていることから保持能を超えてしまっている可能性が考えられます。
長いので一度まとめます。
考察
フィルターに添加する溶解バッファーの量を増加(0.44mL → 2mL)させると、環境DNAの収量が劇的に増加しました。
環境DNAマニュアル記載の方法で収量が少なかった理由としては、図6A, Bのように溶解バッファーがフィルターと十分に接触せずうまく溶解ができていなかった可能性があることが挙げられます。

また、Protocol3のアウトレット側からの逆洗で抽出する方法で、環境DNAの収量がさらに増加(Fig.1 B)したことから、Sterivexカートリッジの細孔に閉じ込められて、うまく溶解されていない環境DNAが存在するかもしれません。
ですが、高濃度群では逆洗しても環境DNA量は増加しませんでした(図1A)。
これについては、カラム保持能の検証結果により説明ができるかもしれません。
Inputされる環境DNAの濃度が高い場合、連結したカラムの下側(Lower)で捕捉され(図2A)、連結した各カラムの環境DNA含有量は単一で抽出したカラムの含有量と類似していたことから、高濃度だとDNeasyのカラムの最大許容量を超えてしまっていたのではないかと考えられます。
抽出溶液のDNA量を計測したところ、DNeasyのカラムは数十μgのDNA保持能力があるにも関わらず、0.4ng – 1.2ngとDNeasyのカラムの規定容量よりも低い測定値が得られました。
この理由としては、環境サンプル中の未知の化合物や汚染物質がシリカ表面への非特異的に結合して、環境DNAの結合の競合または、結合を阻害を発生させている可能性があます。野外サンプル中には、プランクトンや藻類、糞便や分解された腐敗物などが豊富なため、これらのDNAや非特異的な結合によってDNeasyのカラムは保持能の限界を超えてしまう可能性があります。
これらの結果は、定量PCRによってサンプル中の環境DNA量を推定、またはメタバーコーディングで種構成を推定するためには、抽出段階で内部標準による抽出効率をモニタリングする必要性があることも示唆しています。
Part1は以上です。
免責事項
画像はジャーナルのCC BYに従う形で、記事で紹介したオープンアクセスの論文中の画像または、自身で作成したものを使用しています。
十分注意は払っていますが、本記事の情報・内容について保証されるものではありません。また、本記事の利用や閲覧によって生じたいかなる損害について責任を負いません。そして、本記事の情報は予告なく変更される場合がありますので、ご理解くださいますようお願い申し上げます。






